Скачать презентацию на тему водород. Презентация на тему "водород"
9 класс
Учитель: Смирнова Екатерина Сергеевна
Тема урока: Водород.
Цель урока: активизировать и систематизировать знания о нахождение в природе. Физические свойства. Химические свойства водорода:
реакции с неметаллами и металлами. Реакции водорода с оксидами металлов. Получение водорода в лаборатории и промышленности.
Применение водорода.
(слайд 2)
Тип урока: усвоение новых знаний, умений и навыков, и творческого применения их на практике.
Формы работы: лекция, демонстрация презентации.
Оборудование: проектор, учебник.
Ход урока.
Организационный момент: приветствие, проверка готовности к уроку.
Проверка домашнего задания.
Актуализация опорных знаний.
Фронтальная беседа:
1. Что вам известно о водороде как о простом веществе?
2. Найдите водород в ПС.
3. По положению в ПС о каких свойствах водорода вы можете сказать?
Изучение нового материала.
В диссертации М.В.Ломоносова «О металлическом блеске» в 1745г. впервые было описано получение водорода действием кислоты на железо и другие металлы и была выдвинута гипотеза о том, что водород (горючий пар) представляет собой флогистон.
(слайд 3)
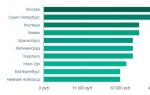
Содержание водорода в земной коре составляет 1% по весу и 17% общего числа атомов. (слайд4)
Водород самый легкий из всех элементов. Он входит в состав воды, которая покрывает около ¾ земной поверхности, в состав многих минералов и горных пород, а также всех органических соединений. В свободном состоянии водород встречается в небольших количествах в верхних слоях атмосферы и в некоторых природных горючих газах. (слайд 5)
Физические свойства . Водород при обычных условиях представляет собой газ без цвета и запаха. Он в 14,5 раза легче воздуха, слабо растворим в воде (в 100 объемах воды растворяется 2 объема водорода). При температуре -253 0 С и атмосферном давлении переходит в жидкое состояние, а при -259 0 С затвердевает. Из-за малой молекулярной массы он легко диффундирует (проходит) через пористые перегородки и даже через нагретую металлическую перегородку. При повышенной температуре водород хорошо растворим во многих металлах (никеле, платине, палладии). (слайд 6)
Водород существует в виде трех изотопов: протия - с массовым числом 1, дейтерия - с массовым числом 2 и трития - с массовым числом 3. Основную часть природного водорода (99,98%) составляет протий. (слайд 7)
Химические свойства.
Атом водорода имеет один электрон. При образовании химических соединений он почти всегда отдает электрон, приобретая заряд +1. Из-за малого заряда ядра атом водорода сравнительно слабо притягивает электроны и может присоединить их только тогда, когда другой элемент легко их отдает. В этом случае атом водорода образует устойчивую двухэлектродную оболочку инертного газа гелия. (слайд 8)
Взаимодействие с щелочными и щелочноземельными металлами.
Щелочные и щелочноземельные металлы легко отдают электроны водороду. Реакция протекает при нагревании металлов в атмосфере водорода и сопровождается образованием солеобразных соединений - гидридов.
2 Na + H 2 = 2 Na H - гидрид натрия
Ca + H 2 = CaH 2 - гидрид натрия (слайд 9)
Взаимодействие с неметаллами.
Более характерны соединения водорода, в которых он проявляет положительную степень окисления, он взаимодействует почти со всеми неметаллами, причем в зависимости от активности неметалла реакция протекает с различной скоростью. Так, с фтором водород взаимодействует всегда со взрывом:
H 2 + F 2 = 2 HF
С хлором он взаимодействует более спокойно. Водород хорошо горит в атмосфере хлора:
H 2 + Cl = 2 HCl
(слайд 10)
Получение водорода в лаборатории.
В лабораторных условиях водород получают:
1) взаимодействием металла с соляной или разбавленной серной кислотой (реакцию проводят в аппарате Киппа):
Zn + 2HCl → ZnCl 2 + H 2
2) взаимодействием со щелочами металла, гидроксид которого обладает амфотерными свойствами (алюминий, цинк):
2Al + 2NaOH + 6H 2 O → 2 Na + 3H 2
Zn + 2KOH + 2H 2 O → K 2 + H 2 ( слайд 11)
3) электролизом воды. Для увеличения электропроводимости воды к ней прибавляют электролит - щелоч или сулфат щелочного металла. Хлориды для этой цели менее пригодны. Так как при их разложении на аноде выделяется хлор.
Получение водорода в промышленности.
1) как побочный продукт при производстве хлора и гидроксидов щелочных металлов методом электролиза растворов их хлоридов;
2) конверсией (превращением) углерода и водяных паров. Для этого в специальных газогенераторах в результате взаимодействия водяных паров с раскаленным углеродом (углем) получают смесь водорода с монооксидом углерода:
C + H 2 O = CO + H 2
Образующуюся газовую смесь вместе с парами воды пропускают над раскаленным монооксидом железа, играющим роль катализатора:
СО + H 2 O = СО 2 + H 2 ,
А затем - через воду или раствор щелочи для поглощения СО 2 ;
3) конверсией метана с водяным паром, углекислым газом или смесью водяных паров и углекислого газа:
CH 4 + СО 2 = 2CO + 2H 2
CH 4 + H 2 O = CO + 3H 2
3CH 4 + СО 2 + 2H 2 O = 4CO + 8H 2
Эти процессы протекают при температуре около 1000 0 С. Катализирует их никель с добавками оксидов магния, алюминия и других металлов. (слайд 12)
Применение.
Водород является ценным сырьем для химической промышленности. Его используют для получения аммиака и синтетического метилового спирта, для гидрогенизации твердого топлива и жиров. Значительное количество водорода используется для получения различных металлов и неметаллов (германий, галлий, вольфрам, молибден и др.) в промышленности путем восстановления их оксидов или галогенидов. Используя высокую температуру горения водорода в кислороде, его применяют при резке и сварке металлических конструкций.(слайд 13)
Проверка усвоения знаний.
Выберите верное определение. Физические свойства водорода:
А)газ без цвета и запаха.
Б) он в 16,4 раз легче воздуха.
В) растворим в воде.
2. Дайте названия изотопам водорода:
1Н -
2Н -
3Н -
3. Вставите пропущенные слова.
Атом водорода имеет один _________. При образовании химических соединений он почти всегда ______ электрон, приобретая заряд ___. Из-за ______ заряда ядра атом водорода сравнительно ______ притягивает _______ и может присоединить их только тогда, когда другой элемент легко их отдает. В этом случае ________ водорода образует устойчивую двухэлектродную оболочку ________ _________ _______. (слайд 15)
Итоги урока. Домашнее задание: учить п.19, выполнить задания к параграфу письменно в тетради.
Отгадайте о чём идёт речь Я, газ, легчайший и бесцветный, Неядовитый и безвредный, Соединяясь с кислородом, Я для питья даю вам воду!
Тема урока «Водород» План урока 1. Водород в природе. 2. Историческая справка. 3. Водород – химический элемент. 4. Водород – простое вещество. 5. Получение и собирание водорода. 6. Физические свойства водорода. 7. Применение водорода.
Водород в природе. Первый я на белом свете: Во вселенной, на планете Превращаюсь в лёгкий гелий, Зажигаю Солнце в небе. Гость из космоса пришёл В воде приют себе нашёл! (Объясните смысл этого стихотворения изучив материал учебника нахождение водорода в природе стр. 71)
Нахождение в природе В земной коре Во вселенной
Исторические сведения Водород был известен ещё в XVI веке Теофрасту Парацельсу (1493-1541) Его получали Ван-Гельмонт(1577-1644), Роберт Бойль (1627-1691), Николя Лемери (1645-1715), Михаил Васильевич Ломоносов (1711-1765), Джозеф Пристли и др.
Всё те же открытия. В 1766 году известный английский учёный Генри Кавендиш получил «искусственный воздух» действием цинка на разведённую соляную кислоту. Это было совершенно новое вещество, которое хорошо горело и получило название «горючего воздуха»
Открытие водорода Лишь в 1787 году Антуан Лавуазье доказал, что «горючий воздух»,открытый в 1766 году входит в состав воды и дал ему название «гидрогениум», т.е. «рождающий воду», «водород».
Водород – химический элемент. Характеристика водорода по периодической системе. 1. Порядковый номер. 2. Номер периода. 3. Номер группы. 4. Относительная атомная масса. 5. Валентность водорода.
Водород – простое вещество. Н 2
Водород как простое вещество и как химический элемент Параметры сравнения Химический элемент Простое вещество Химическая формула Н Н 2 Относительная атомная или молекулярная массы A r(H) = 1 M r (H 2) =2 Свойства Входит в состав простых и сложных веществ. Обладает набором физических и химических свойств.
Ответьте на вопрос. Если бы перед вами стояла задача получить большое количество водорода, какое сырьё вы бы выбрали и почему?
Получение водорода из воды с помощью солнечной энергии
Получение водорода В промышленности: 2СН 4 + О 2 = 2СО + 4Н 2 2 H 2 O = 2H 2 + O 2 В лаборатории: Zn + H 2 SO 4 = ZnSO 4 + H 2
Получение водорода в лаборатории
Собирание водорода Методом вытеснения воды Методом вытеснения воздуха
А сейчас - физминутка!
Образование гремучей смеси Обычно лёгок и летуч, Он вдруг становится могуч: Его нагрев неосторожно Взорвать в округе всё возможно.
Физические свойства водорода Лёгкий горючий газ без цвета, запаха и вкуса. Температура плавления -259,15 Температура кипения -252,7 Плохо растворим в воде.
Некоторые области применения водорода
Применение водорода Водородом заполняли дирижабли вплоть до 1937 года, пока не взорвался немецкий дирижабль «Гинденбург». Погибло 36 человек. Размеры дирижабля достигали размеров двух футбольных полей.
Водород в качестве горючего
Водород – аккумулятор энергии
Если вы согласны с утверждениями, поставьте плюс. 1. Я узнал много нового и интересного. 2. На все возникшие в ходе урока вопросы я получил ответы. 3. Мне это пригодится в будущей профессиональной деятельности и в повседневной жизни. 4. Считаю, что работал добросовестно и достиг цели урока.
Спасибо за урок! Запишите домашнее задание. Стр.71 – 74(читать) Подготовить сообщения по темам: «Водород во Вселенной», «Старинные способы получения водорода», «Из истории развития воздухоплавания».
Цель: систематизация знаний учащихся о водороде.
Задачи:
- Обучающие : привести в систему знания учащихся о водороде; закрепить умения применять полученные знания при объяснении новых фактов; продолжить формирование умения составлять формулы веществ, уравнения реакций на основании знания степени окисления элементов.
- Развивающие : развивать мышление учащихся, умение анализировать, сравнивать, обобщать, наблюдать, запоминать, работать в нужном темпе, осуществлять самоконтроль; формировать общеучебные умения и навыки.
- Воспитательные : воспитывать личностные качества, обеспечивающие успешность исполнительной деятельности (дисциплинированность, ответственность), творческой деятельности (активность, увлечённость, наблюдательность, сообразительность, способность к самооценке).
Методы, методические приёмы. Беседа с учащимися, работа с инструктивными картами и материалами слайдов, демонстрационный эксперимент, частично-поисковый метод.
Реактивы. Цинк, соляная кислота, оксид меди (II).
Оборудование. Раздаточный дидактический материал, таблица химических элементов Д.И. Менделеева, шкатулка, компьютер, медиапроектор; спиртовка, спички, пробирки, лабораторные штативы, кристаллизатор.
Ход урока
I. Мотивация. Актуализация знаний
Учитель: Сколько всего известно химических элементов?
Ученик: 110.
Учитель: Сколько химических элементов входит в состав веществ, образующих клетки всех живых организмов?
Ученик: более 70.
Учитель: Основу жизни составляют 6 элементов первых трёх периодов (Н, С, N, О, Р, S), на долю которых приходится 98% массы живого вещества. Один из них мы сегодня будем изучать. А вот какой именно мы узнаем из загадок в шкатулочке.
Загадки
- Первый я на белом свете:
Во Вселенной, на планете,
Превращаюсь в лёгкий гелий,
Зажигаю солнце в небе.
- Гость из космоса пришёл,
В воде приют себе нашёл.
Неядовитый и безвредный.
Соединяясь с кислородом,
Я для питья даю вам воду.
Ученик: Водород.
Учитель: Итак, тема урока: Водород. (слайд 1 . См. Приложение)
II. Изучение нового материала
Учитель: Сейчас вы отправитесь в путешествие, чтобы познакомится с удивительным химическим элементом – водородом – и образованным им простым веществом. Для этого вам понадобится карточка-путеводитель. Внимательно рассмотрите её и скажите, где вы сегодня побываете и что узнаете.(слайд 2)
Карточка-путеводитель
| Название станций | Книга жалоб и предложений | Спец. пометки |
| “Открытие водорода” | v
– это я знаю + – новая информация ! – это интересно |
|
| “Распространение водорода” | ||
| “Получение водорода” | ||
| “Применение водорода” | ||
| “Выбери задание” | ||
| “Тест” | ||
| “Кроссворд” |
Ученики: Называют станции, формулируя при этом цели и задачи урока.
Учитель: На каждой станции есть книга жалоб и предложений, где вы должны поставить специальные пометки. (слайд 3 )
Станция 1: “Открытие водорода” (сообщение ученика )
Учитель: Внимательно послушайте сообщение и ответьте на вопрос: “Кто и когда открыл водород?”
Открытие водорода:
гидрогениум, вода род.
(слайд 4 )
(формула метана?),
(слайд5, слайд 6 – проверка задания )
Порядковый номер:
Период:
Группа:
Подгруппа:
Электронная формула атома:
Учитель: Почему водород поместили и в 1 группу главную подгруппу и в 7 группу главную подгруппу Периодической системы.
Ученик: Водород может проявлять и окислительные и восстановительные свойства.
Учитель: Степень окисления у водорода чему равна?
Ученик: +1, -1, 0.
Учитель: Молекула водорода состоит из двух атомов и образована ковалентной неполярной химической связью.
(слайд 7 )
Вкус:
Цвет:
Запах:
Температура кипения:
Растворение в воде:
(слайд 8 )
Химические свойства водорода:
1) + неметалл:
2Н 2 + О 2 = 2Н 2 О
Н 2 + Сl 2 = 2HCl
H 2 + S = H 2 S
3H 2 + N 2 = 2NH 3
2) + металл:
H 2 + 2Na = 2NaH
H 2 + Ca = CaH 2
Учитель: Как вы думаете со сложными веществами водород будет реагировать? И с какими?
Ученик: С основным оксидом.
Учитель: (демонстрационный опыт: CuO + H 2 = H 2 O + Cu)
Ученик: записывает уравнение реакции определяет окислитель и восстановитель методом электронного баланса.
(слайд 9, слайд 10 – проверка задания )
Получение водорода:
1) В лаборатории:
Zn + HCl = ZnCl 2 + H 2
2) В промышленности:
С + Н 2 О = СО + Н 2
СН 4 + Н 2 О = СО + Н 2
Н 2 О = Н 2 + О 2
(слайд 11 )
III. Первичная проверка усвоения знаний.
Станция 8: “Выбери задание”
Задания минимального уровня (проверка заданий устно).
2. На каком рисунке (а или б ) отображен способ "переливания" водорода из одного сосуда в другой? Ответ поясните.

Задания общего уровня (проверка заданий устно и у доски)
А) с углём;
Б) с метаном.
Задания продвинутого уровня (проверка заданий устно и у доски)
IV. Закрепление знаний
Станция 9: “Тест”
1) Cu + HCl;
2) Zn + HCl;
3) Cu + H 2 O;
4) S + NaOH
1) I;
2) II;
3) III;
4) V
1) чугун;
2) водород;
3) соляная кислота;
4) воздух.
4. Водород не реагирует с:
1) N 2 ;
2) S;
3) O 2 ;
4) HCl
1) железа с водой;
2) натрия с водой;
3) оксида кальция с водой;
1) HCl;
2) 2HCl;
3) 3HCl;
4) 4HCl
8. Водород реагирует:
4) только с неметаллами.
9. Водород реагирует с:
1) Н 2 О;
2) SO 3 ;
3) Cl 2 ;
4) Au
1) метана с водой;
2) железа с водой;
3) электролизом воды;
4) цинка с соляной кислотой.
Ученики: выполнив задание, меняются тетрадями друг с другом, проверяют и выставляют оценки.
Учитель: Правильные ответы:
Станция 10: “Кроссворд” (резерв )

V. Подведение итогов урока
Фронтальная беседа/
VI. Информация о домашнем задании
(слайд 13 )
Учитель: параграф 17; упр. № 3,4 на стр.103.
Литература
- Габриелян О.С . Химия. 9 кл.: рабочая тетрадь к учебнику О.С.Габриеляна “Химия. 9 класс”/ О.С.Габриелян, А.В.Яшукова. – 6-е изд., стереотип. – М.: Дрофа, 2007.
- Габриелян О.С . Химия. 9 класс: учеб. для общеобразоват. Учреждений/ О.С.Габриелян. – 12-е изд., стереотип. – М.: Дрофа, 2007.
- Горковенко М.Ю . Химия. 8 класс: Поурочные разработки к учебникам О.С.Габриеляна; Л.С.Гузея, В.В.Сорокина, Р.П.Суровцевой; Г.Е.Рудзитиса, Ф.Г.Фельдмана. – М.: ВАКО, 2004.
- Гузей Л.С. и др. Химия. 8 класс: учеб для общеобразоват. учреждений/ Л.С.Гузей, В.В.Сорокин, Р.П.Суровцева. – 6-е изд., перереб. и доп. – М.: Дрофа, 2001.
- Единый государственный экзамен 2001: Тестовые задания: Химия/ М.Г.Минин, Н.С.Михайлова, В.Ф.Гридаев и др.; М-во образования РФ. – 2-е изд. – М.: Просвещение, 2002.
- Катаева Л.Г., Толкачева Т.К . Химия: Карточки-задания по неорган. химии: 8 кл.: Кн. для учителя. – М.: Просвещение, 1998.
- Научно-теоретический и методический журнал “Химия в школе”, №10 2002год, №3 2004 год, №4 2008 год.
- Суровцева Р.П . Химия. 8 кл.: Поурочные разработки с дидактическим материалом к учебнику Л.С.Гузея, В.В.Сорокина, Р.П.Суровцевой “Химия. 8”/ Р.П.Суровцева, М.И.Виноградова. – 2-е изд., стереотип. – М.: Дрофа, 2004.
- Течсты по химии. – 8-9 кл.: Учебно-метод. Пособие/ Р.П.Суровцева, Л.С.Гузей, Н.И.Останний, А.О.Татур. – 4-е изд., стереотип. – М.: Дрофа, 2000.
- Учебно-методическая газета для учителей “Химия” Издательский дом “ Первое сентября”: №10, 24 2008 год: № 2 2009 год.
Раздаточный материал
Карточка-путеводитель
| Название станций | Книга жалоб и предложений | Спец. пометки |
| “Открытие водорода” | v
– это я знаю + – новая информация - – информация, противоречащая моим знаниям ? – информация требует пояснения ! – это интересно |
|
| “Распространение водорода” | ||
| “Визитка химического элемента” | ||
| “Физические свойства простого вещества” | ||
| “Химические свойства простого вещества” | ||
| “Получение водорода” | ||
| “Применение водорода” | ||
| “Выбери задание” | ||
| “Тест” | ||
| “Кроссворд” |
Станция 2: “Распространение водорода”
Время стоянки 3 мин. Прочтите текст и ответьте на вопрос: Почему водород самый первый, но второй?
По распространенности в нашей Вселенной водород занимает первое место. На его долю приходится около 92% всех атомов (8% составляют атомы гелия, доля всех остальных вместе взятых – менее 0,1%). Таким образом, водород – основная составная часть звезд и межзвездного газа. В условиях звездных температур (например, температура поверхности Солнца – 6000 °С) и межзвездного пространства, пронизанного космическим излучением, этот элемент существует в виде отдельных атомов.
Массовая доля водорода в земной коре составляет 1% – это девятый по распространенности элемент. Однако его роль в природе определяется не массой, а числом атомов, доля которых среди остальных элементов составляет –17% (второе место после кислорода, доля атомов которого равна –52%). Поэтому значение водорода в химических процессах, происходящих на Земле, почти так же велико, как и кислорода.
В отличие от кислорода, существующего на Земле и в связанном, и в свободном состоянии, практически весь водород на Земле находится в виде соединений; лишь в очень незначительном количестве водород в виде простого вещества имеется в атмосфере (0,00005% по объему).
Основным соединением водорода является вода. Кроме того, большое его количество входит в состав многочисленных соединений с углеродом (органических веществ), составляющих основу нефти, природного газа (формула метана?), угля и др. Он непременная составная часть веществ, образующих живые организмы (–6,5% от сухой массы).
Станция 3: “Визитка химического элемента”
Время стоянки 3 мин. Работая в паре, определите место положения элемента в Периодической системе, составьте электронную формулу атома. Сделайте записи в тетради:
Порядковый номер:
Период:
Группа:
Подгруппа:
Электронная формула атома:
Станция 4: “Физические свойства простого вещества”
Время стоянки 3 мин. Работайте в парах. Запишите в тетради физические свойства простого вещества по рисунку на слайде:
Вкус:
Цвет:
Запах:
Температура кипения:
Растворение в воде:
Станция 5: “Химические свойства простого вещества”
Время стоянки 15 мин. Работайте в парах. Запишите в тетради химические свойства водорода. У подчёркнутых уравнений реакций определите окислитель и восстановитель методом электронного баланса.
Химические свойства водорода:
1) + неметалл:
2Н 2 + О 2 = 2Н 2 О
Н 2 + Сl 2 = 2HCl
H 2 + S = H 2 S
3H 2 + N 2 = 2NH 3
2) + металл:
H 2 + 2Na = 2NaH
H 2 + Ca = CaH 2
Станция 6: “Получение водорода”
Время стоянки 3 мин. Работайте в парах. Запишите в тетради получение водорода. Расставьте коэффициенты в уравнениях реакций.
Получение водорода:
1) В лаборатории:
Zn + HCl = ZnCl 2 + H 22) В промышленности:
С + Н 2 О = СО + Н 2
СН 4 + Н 2 О = СО + Н 2
Н 2 О = Н 2 + О 2
Станция 7: “Применение водорода”
Время стоянки 1 мин. Работайте в парах. Запишите в тетради применение водорода, используя материал учебника рис.46, стр.101.
Станция 8: “Выбери задание”
Время стоянки 4 мин. Работайте самостоятельно. Выберите только те задания,
С которыми вы справитесь (по выбору):
Задания минимального уровня
1. Мыльные пузыри, наполненные водородом, поднимаются вверх. Объясните это явление.
2. На каком рисунке (а или б ) отображен способ "переливания" водорода из одного сосуда в другой? Ответ поясните.
Задания общего уровня
Запишите уравнения реакций получения водорода конверсией водяных паров:
А) с углём;
Б) с метаном.
Задания продвинутого уровня
Запишите уравнения реакций следующих переходов: Н 2 SO 4 – Н 2 – Н 2 О – КОН
Станция 9: “Тест”
Время стоянки 5 мин. Работайте самостоятельно. Выберите один правильный ответ:
1. Водород является продуктом взаимодействия:
1) Cu + HCl;
2) Zn + HCl;
3) Cu + H 2 O;
4) S + NaOH
2. Укажите валентность фосфора в водородном соединении:
1) I;
2) II;
3) III;
4) V
3. Индивидуальным веществом является:
1) чугун;
2) водород;
3) соляная кислота;
4) воздух.
4. Водород не реагирует с:
1) N 2 ;
2) S;
3) O 2 ;
4) HCl
5. Химические свойства водорода используются при:
1) получении сверхнизких температур;
2) наполнении стратостатов и шаров-зондов;
3) получении металлов из их оксидов;
4) отводе теплоты в электрических машинах.
6. Водород в лаборатории получают взаимодействием:
1) железа с водой;
2) натрия с водой;
3) оксида кальция с водой;
4) цинка с соляной кислотой.
7. Формула продукта реакции и коэффициент перед ней в уравнении реакции взаимодействия водорода с хлором:
1) HCl;
2) 2HCl;
3) 3HCl;
4) 4HCl
8. Водород реагирует:
1) только с простыми веществами;
2) с простыми и сложными веществами;
3) только со сложными веществами;
4) только с неметаллами.
9. Водород реагирует с:
1) Н 2 О;
2) SO 3 ;
3) Cl 2 ;
4) Au
10. В промышленности водород не получали и не получают взаимодействием:
1) етана с водой;
2) железа с водой;
3) электролизом воды;
4) цинка с соляной кислотой.
Станция 10: “Кроссворд”
Время стоянки 3 мин. Работайте в парах.
Ключевым словом является название ближайшей к Земле звезды, на которой преобладает химический элемент водород. Каждое предложенное химическое явление подтвердите соответствующими уравнениями химических реакций.

- Сложные вещества, при взаимодействии которых с водородом получают металлы.
- Вещество, которое образуется при горении водорода в кислороде.
- Кислоты, состоящие из атомов водорода и другого химического элемента.
- Кислота, которая легко разлагается на оксид углерода (IV) и воду.
- Металл, непосредственно взаимодействующий с водородом.
- Кислота, по уровню производства которой можно судить о мощности химической промышленности страны.
Сообщение учащегося
Открытие водорода:
Английский ученый Генри Кавендиш в 1766 г. получил водород действием цинка, олова или железа с серной или соляной кислотой. Водород до Кавендиша получали и другие ученые, но они и не пытались изучить его свойства. Интересно отметить, что водород принимали за разновидность воздуха или флогистон. Ломоносов в своей диссертации “О металлическом блеске” писал: “При растворении какого-либо неблагородного металла, особенно железа, в кислотных спиртах из отверстия склянки вырывается горючий пар, который представляет собой флогистон”.
Большинство исследователей, в том числе и Кавендиш, принимали водород за флогистон, и называли его “горючий газ”. Кавендиш первым подробно описал способы получения, а так же физические и химические свойства водорода. Он установил, что водород не растворяется в воде и щелочах, при смешивании его с воздухом образуется взрывчатая смесь. Поэтому Кавендиш новому газу дал название “горючий воздух”. Поскольку при действии кислот на различные металлы выделялся один и тот же газ, Кавендиш утвердился в своем мнении что водород – это флогистон. В 1781 году английский ученый, наблюдая горение водорода на воздухе: Н 2 + О 2 = 2Н 2 О установил, что водород при горении превращается в чистую воду. Но он сделал неверный вывод, посчитав, что вода, вещество элементарное, т.е. простое. В 1783–1784 гг. А. Лавуазье совместно с Ж. Менье осуществили термическое разложение воды и установили, что она состоит из кислорода и водорода.
Данные Лавуазье: 85 частей кислорода и 15 частей водорода.
Современные данные: 88,9% кислорода и 11,2% водорода.
Современное название водороду дал французский физик и химик А. Гитон де Морво в 1787 году. Он предложил латинское название гидрогениум, означающее “рождающий воду”. Русское название (по смыслу такое же): вода род.
Водород стал первым известным простым газообразным веществом. Его открытие имело огромное значение для становления современной научной химии.
Загадки
Первый я на белом свете:
Во Вселенной, на планете,
Превращаюсь в лёгкий гелий,
Зажигаю солнце в небе.Гость из космоса пришёл,
В воде приют себе нашёл.Я, газ легчайший и бесцветный,
Неядовитый и безвредный.
Соединяясь с кислородом,
Я для питья даю вам воду.
Цель и задачи урока: Образовательные: формировать представления о водороде как химическом элементе и простом веществе; расширить знания об областях применения водорода. Развивающие: развивать самостоятельность мышления, развивать интеллектуальные умения (анализировать, сравнивать, устанавливать причинно-следственные связи, работать по аналогии, выдвигать предположения). Воспитательные: формировать научное мировоззрение, экологическое мышление, воспитывать культуру общения.

Тест «Да-Нет-ка» 1 - Водород означает «кислотырождающий» (нет) 2 - Самый распространенный во Вселенной (да) 3 - Его валентность равна - II (нет) 4 - В лаборатории получают при взаимодействии металлов с кислотами. (да) 5 - Впервые получен Ж. Пристли. (нет) 6 - Легче воздуха в 14,5 раз (да) 7 - Взаимодействует с металлами и неметаллами. (да) 8 - Простое вещество водород имеет формулу Н. (нет) 9 - Восстанавливает металлы из оксидов. (да) 10 - При горении образует много энергии. (да)











Презентация к уроку
«Водород и его свойства»
8 класс
Чаплыгина Ираида Ивановна

«НИ ОДНА НАУКА НЕ НУЖДАЕТСЯ В ЭКСПЕРИМЕНТЕ В ТАКОЙ СТЕПЕНИ КАК ХИМИЯ»
(МАЙКЛ ФАРАДЕЙ)

Загадка
Вы со мной уже встречались
Я космический скиталец,
Элементов прародитель
И отважный предводитель
Я любитель кислорода
Вместе с ним даю я воду.

Станция «ПОЛУЧЕНИЕ ВОДОРОДА»


Станция «ПОЛУЧЕНИЕ ВОДОРОДА»


Ответ варианта №1
- Водород находится в первой группе. Порядковый номер 1, валентность равна 1.
- H, H2
Молекулярная масса равно 2, атомная – 1;
Молярная масса 2г/моль
Ответ варианта №2

Станция «ПОЛУЧЕНИЕ ВОДОРОДА»




Станция «ПОЛУЧЕНИЕ ВОДОРОДА»


Станция «ПОЛУЧЕНИЕ ВОДОРОДА»
ZnCl2+H2


Тест
- Это вещество является газом;
- Газ, без цвета, без запаха, мало растворим в воде;
- Самый распространенный элемент в космосе;
- Самый распространенный химический элемент в земной коре;
- Химический элемент, которой входит в состав воды;
- Молекула, состоит из двух атомов;
- Из каких веществ получают кислород и водород:
А) цинк и соляная кислота, калий и вода; разложением воды;
Б) перманганат калия нагревали; переоксид водорода, разложением воды.

Определить и выписать номера только верных утверждений
Водород
Кислород
примечание

Домашнее задание
Упр.1-2, с.76
Минисообщение «Применение водорода»

ЗАГАДКИ
- 1. ГОСТЬ ИЗ КОСМОСА ПРИШЕЛ,
В ВОЗДУХЕ ПРИЮТ СЕБЕ НАШЕЛ.
- 2. КАКИЕ ХИМИЧЕСКИЕ ЭЛЕМЕНТЫ УТВЕРЖДАЮТ,
ЧТО МОГУТ ДРУГИЕ ВЕЩЕСТВА РОЖДАТЬ.